医療機器受託製造業者とは
-
医療・福祉

2025年3月7日
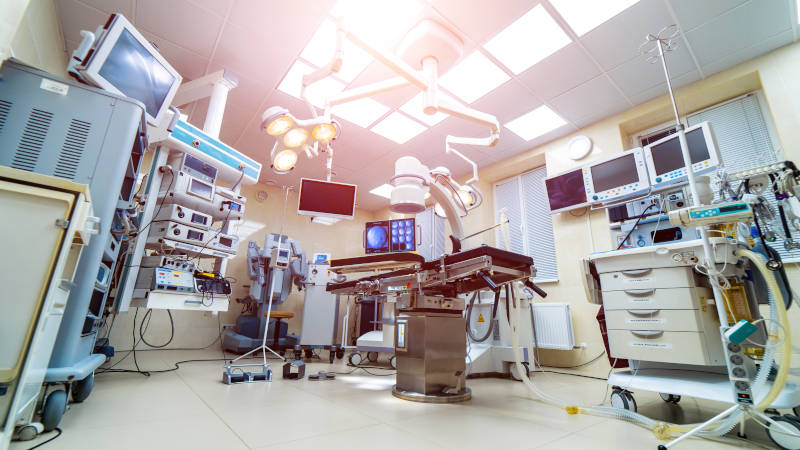
ある報告書によれば、世界の医療機器市場は2023年に5,184億6,000万米ドル、2032年には8,868億米ドルに成長すると予測されています*1。また医療技術も急速に進歩しています。このような中、医療機器受託製造業者の役割はますます重要になっています。医療機器受託製造業者は、医療機器メーカーが高品質で規格に適合した医療機器を効率よく市場に投入できるよう、多岐にわたるサービスを提供しています。 ここでは、医療機器受託製造業者の典型的な役割を詳しく見ていき、記事の後半では当社が医療機器受託製造業者として行う業務の一部をご紹介します。
なお、文中に出てくる専門用語は、ページ末尾の「用語説明」で詳しく説明しています。
医療機器委託製造業者の役割と仕事
医療機器の製造業者は、完成した機器を設計・製造・製作・組立、または処理する業者となります。この中で、医療機器委託製造業者は、製造業者との取り決めに従って、委託された製造作業(製造、加工、包装、保管、試験などの一部または全部の委託)を行う業者です。さらに、委託された内容には製造を行うための設計的な改善が含まれることもあります。また、医療機器委託製造業者が機器の設計を含むかどうかは、国によって少し異なります。日本の薬機法では、製造業者には設計・主たる組立て・最終製品の保管・滅菌の区分があり、それらの一部または全部を委託することが考えられますので、すなわち医療機器委託製造業者は設計を含む可能性があります。一方で、米国のFDAでは、製品仕様を開発する施設は仕様開発者と呼ばれ、医療機器委託製造業者とは区別されています。
設計・開発
市場およびお客様のニーズと期待に基づいて作成された要求仕様書および設計計画書をインプットとして、医療機器に求められるリスクマネジメント*2、ユーザビリティエンジニアリング*3、ソフトウェアライフサイクルプロセス*4、サイバーセキュリティ*5、安全規格*6などの規格要求に準拠して設計・開発を行います。そして、検証および妥当性確認を通じて、医療機器が必要な要求事項を全て満たし、量産の準備が整っていることを確認します。
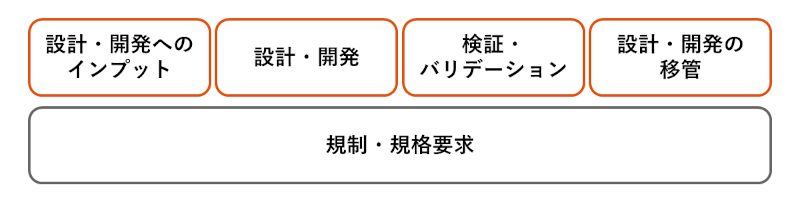 医療機器受託製造の設計・開発段階で実施する項目の概念図
医療機器受託製造の設計・開発段階で実施する項目の概念図
生産
医療機器および必要数量などに応じた最適な工程設計や設備設計を行い、リスクマネジメント*2、プロセスバリデーション*7およびソフトウェアバリデーション*8などを通じて、適切な製造工程を実現します。また、購入部品のサプライヤーの選定および調達から医療機器の組み立て・ラベリング・梱包・最終保管に至るまで、医療機器の品質と安全性を確保するために適切な生産管理を行います。生産管理は次のものを含んでいます。
- 不適合製品および未完成品の市場への流出を防ぐための識別管理および不適合品管理
- 万が一市場で不適合製品が発見された場合の、医療機器に対する修正・是正処置を決定するために行う影響範囲の分析に必要な、様々なデータを含むトレーサビリティ管理
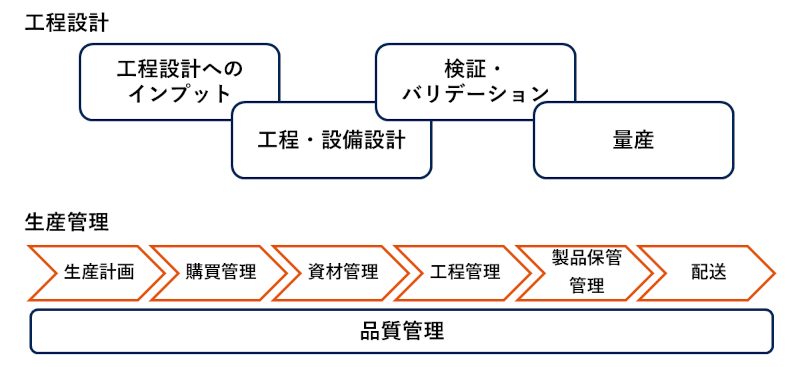 医療機器受託製造の生産段階で実施する項目の概念図
医療機器受託製造の生産段階で実施する項目の概念図
製品の清浄性・汚染管理
滅菌医療機器には固有の要求がありますが、通常の医療機器についても、その製品特性上、製品の清浄性および汚染管理といった衛生管理が必要です。
汚染管理には、製品を取り扱う作業者への汚染管理と市場への汚染拡大防止の2つの側面があり、その点も考慮した生産管理および附帯サービス活動を行う必要があります。
附帯サービス
附帯サービスは、継続的な製品使用の支援と顧客満足度の向上を目的とした戦略的な活動です。
継続的な製品使用を支援する観点では、市場における医療機器の品質および安全性を維持するため、設置、返品・修理およびサービスパーツの提供を行います。また、保守点検が必要な医療機器に対しては、保守点検サービスを提供します。一方、顧客満足度の向上の観点では、技術的アドバイス、ユーザートレーニングなども行います。
 医療機器受託製造の付帯サービスとして実施する項目の概念図
医療機器受託製造の付帯サービスとして実施する項目の概念図
規制要求への遵守
医療機器受託製造会社の最も重要な機能の一つは、規制要求に対する遵守です。米国のFDAや欧州のMDR、日本の薬機法など、医療機器を販売する国ごとにさまざまな規制要求があり、その内容に遵守した医療機器を設計・製造する必要があります。
ASPINAが行う医療機器受託製造業者の業務
設計・開発
ASPINAの設計・製造能力は、さまざまな市場で数多くの長期的なパートナーから信頼されています。当社は40年以上にわたり医療用製品を提供してきました。これには部品、モジュールアセンブリ、日本市場向けのポケット型補聴器などの完成品の設計・製造が含まれます。ASPINAは、機器の性能や耐久性、コスト競争力を向上させるため、新しい技術的な考え方や手法を用いて積極的に開発しています。
生産
ASPINAには日本、中国、メキシコに生産拠点があり、効果的なサプライチェーンマネジメントをベースに部品の現地調達化を推進しています。また、医療機器分野だけでなく自動化、環境、車載分野向けの製品でも使用する部品をまとめて大量に購入しているため、部品調達コストを抑えた製品提供が可能です。
附帯サービス
日本向け医療機器のポケット型補聴器において、返品・修理およびサービスパーツ提供の取り組み実績があり、お客様の相談に柔軟に対応できます。
規制要求に対する遵守
日本向けの医療機器を製造するために必要な医療機器製造業(設計・主たる組立て・最終製品の保管)の登録を行っています。また、ポケット型補聴器を日本で製造販売するために、第二種医療機器製造販売業およびポケット型補聴器の製造販売認証を取得しています。さらに、規制要求と連携した医療機器の品質マネジメントシステムの国際規格「ISO13485」を日本国内の一部製品の設計、製造において取得しており、規制要求に遵守した対応の経験もあります。現在、FDAの規制要求に対応した仕組みの構築に取り組んでおり、将来的には日本以外の生産拠点への展開も考えています。
医療機器製造の頼れるパートナー ASPINA
医療機器受託製造企業は、医療技術産業において欠くことのできないパートナーです。設計・開発から製造、包装、附帯サービスに至るまで、医療機器のライフサイクル全体を支える包括的なサービス群を提供しています。ASPINAを活用することで、医療機器メーカーは技術革新に集中でき、最先端の医療ソリューションを市場に提供することが可能となります。ASPINAは、革新的で最先端の医療機器の開発に取り組む医療機器メーカーを包括的に支援します。お困りごとがありましたらお気軽にお問い合わせください。
関連情報
用語説明
- *2 リスクマネジメント
- リスクとは、危害(人の受ける身体的障害若しくは健康障害、または財産若しくは環境の受ける害)の発生確率と重大さの組み合わせであり、設計・開発のみならず、購買、製造、検査など、医療機器の構想設計から廃棄までのライフサイクル(人生と同じ)全般において、予見可能なさまざまな要因(使用目的以外での使用、輸送時の落下、高温下での保管など)により、医療機器が正しく動作しないことによるリスクが考えられます。このリスクには、受容できるリスク(発生確率、または重大さが低く、無視できるなど)と受容できないリスクがあります。このリスクを医療機器のライフサイクル全般において抽出し、受容できないリスクがある場合には、事前にその対策を行うことにより、安全な医療機器を市場に届けることができます。これは予防処置の一つとなります。
- *3 ユーザビリティエンジニアリング
- ユーザビリティエンジニアリングは、ユーザーのミスによって引き起こされる医療エラーを防ぐためのリスク管理が含まれます。このプロセスはユーザーの視点に立ち、想定するユーザーが安全かつ効果的に使用できるように医療機器を設計するものです。
- *4 ソフトウェアライフサイクルプロセス
- ソフトウェアライフサイクルプロセスは、ソフトウェア開発のための一連のプロセスであり、ソフトウェアの安全性を確保するためのリスク管理プロセスを含みます。ソフトウェアモジュールが不具合を起こす予見可能な要因(センサが故障する、ある条件で正しい測定が出来ないなど)に対するリスクの度合いに応じて、設計プロセスと対策を実施します。
- *5 サイバーセキュリティ
- サイバーセキュリティには、不正アクセスやサイバー脅威を防ぐための対策による、プログラムとデータを保護するためのリスク管理があります。またソフトウェアライフサイクルプロセスと密接に関連しています。
- *6 安全規格
- 落下・衝撃、電磁波、熱などの外的要因が発生しても、医療機器の基本性能の維持および安全性を維持することが求められます。基本性能とは、想定される外的要因や使用の範囲内では維持されなければならない必須の性能(患者監視アラーム機能、患者検査機能、薬品投与機能など)です。
- *7 プロセスバリデーション
- 工程や設備が仕様通りに稼働するようにするためのバリデーション(テストによる確認)です。これには、あらかじめ定められた品質基準を満たす製品を一貫して生産できる工程であることをテストし、確認することが含まれます。
- *8 ソフトウェアバリデーション
- 医療機器の品質マネジメントシステム、製造工程および監視機器・測定機器で使用するソフトウェアがその役割を適切に果たせるようにするためのバリデーション(テストによる確認)です。これには、これらのソフトウェアが適切に機能し信頼できるかをテストし、確認することが含まれます。